全文轉載自“iNature”公眾微信號
細胞外囊泡(EVs)在臨床治療中有多種應用。然而,目前分離血漿EVs的技術存在程序繁瑣和產量有限的問題。
2022年11月20日,南方醫(yī)科大學李博、陳金香及鄭磊共同通訊在Journal of Extracellular Vesicles(IF=17)在線發(fā)表題為“Rapid and efficient isolation platform for plasma extracellular vesicles: EV-FISHER”的研究論文,該研究開發(fā)了一種血漿胞外囊泡的快速高效分離平臺:EV-FISHER。該平臺由具有可裂解脂質探針(PO43?-間隔物-DNA-膽固醇,PSDC)。EV-FISHER 通過膽固醇從血漿中引誘EVs,并用普通離心機將它們分離。捕獲的EVs可以在隨后通過脫氧核糖核酸酶I切割PSDC時釋放和收集。
EV-FISHER 在時間(40-240 分鐘)、隔離效率(74.2%-18.1%)和隔離要求(12,800 g-135,000 g)方面明顯優(yōu)于超速離心(UC)。除了在血漿中的穩(wěn)定性能外,EV-FISHER還表現(xiàn)出與下游單EV流式細胞術的出色兼容性,能夠鑒定glypican-1(GPC-1)EVs,用于乳腺癌隊列的早期診斷,臨床階段分化和治療效果評估。這項工作描繪了一種有效的策略,將EVs從復雜的生物體液中分離出來,具有促進基于EVs的治療診斷學的潛力。

細胞外囊泡(EVs)是由所有類型的細胞以進化保守的方式釋放的磷脂雙層包圍的顆粒,范圍在30到1000納米之間。越來越多的證據(jù)表明,EVs在細胞間通信、疾病發(fā)展和進展中發(fā)揮著重要作用。特別是EVs攜帶豐富的生物分子,如蛋白質、核酸、脂類等,具有作為下一代生物標志物的極好潛力。然而,大小不一的EVs存在于生物液體中,例如血漿、血清、尿液和唾液,其中非EVs生物分子占主導地位。
因此,開發(fā)一種有效的方法將EVs從復雜流體(如血漿)中分離出來是一項艱巨的挑戰(zhàn)。目前,從血漿中分離EVs最常用的方法是差分超速離心(UC)。然而,UC是耗時的,并且會同時分離蛋白質聚集物等污染物。因此,如何以臨床友好的方式分離出產量較高的血漿EVs仍然是一個挑戰(zhàn)。
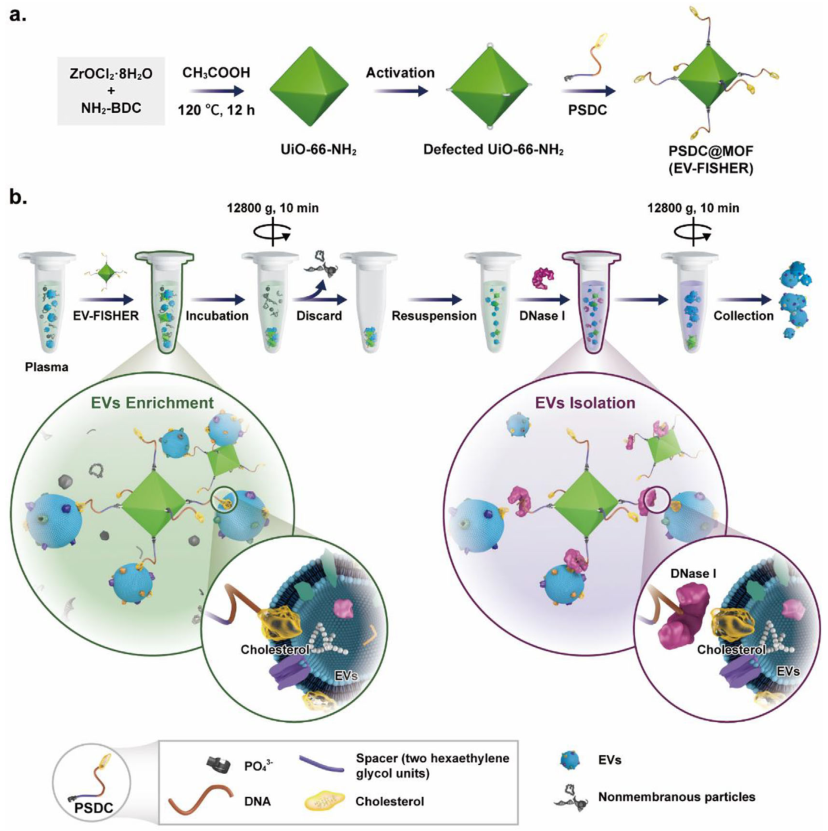
EV-FISHER合成示意圖和血漿EVs分離工作流程示意圖(圖源自Journal of Extracellular Vesicles )
最近,一種脂質納米探針已被開發(fā)用于靶向EVs的磷脂雙層以促進其分離。與傳統(tǒng)的EVs識別元件相比,脂質納米探針通過靶向EVs的磷脂雙層而不是特定的表面生物大分子(CD63,CD9,磷脂絲氨酸等)捕獲EVs。另外,脂質探針和EVs膜之間強烈的疏水相互作用有望產生有效的結合。
因此,這種基于脂質的策略在分離總EV群體方面具有優(yōu)勢,從而為臨床判斷提供了全面的樣本信息。最近,一個抗體輔助的MOF平臺已經(jīng)被開發(fā)用于 EVs 分離,命名為 Tim4@ILI-01。然而,這種策略仍然需要費力的修改和長時間的隔離(> 2小時)。因此,基于MOFs的快速高效的EVs隔離平臺在很大程度上仍未被開發(fā)。
在此,該研究報告了一個稱為EV-FISHER的MOF平臺,用于EVs 的快速富集和分離。由于這種分離策略的精巧設計,所提出的基于MOF的EV分離平臺可以在可用的商業(yè)試劑的臨床實驗室中重復使用。這項工作為在一般臨床實驗室中快速有效地分離血漿EV以進行下游分析提供了一種有前途的策略。
原文鏈接:
https://onlinelibrary.wiley.com/doi/full/10.1002/jev2.12281
