全文轉(zhuǎn)載自:“醫(yī)學與人文”微信公眾號

為了在生物醫(yī)藥領(lǐng)域大力推進科技創(chuàng)新和產(chǎn)業(yè)化應(yīng)用,實現(xiàn)生物醫(yī)藥技術(shù)惠民,國家先后出臺了《關(guān)于全面推進衛(wèi)生與健康科技創(chuàng)新的指導意見》、《關(guān)于深化審評審批制度改革鼓勵藥品醫(yī)療器械創(chuàng)新的意見》、《“十四五”生物經(jīng)濟發(fā)展規(guī)劃》等一系列政策。2020年我國開展的新藥臨床試驗已經(jīng)超過仿制藥,占比達到57%,說明我國正在實現(xiàn)從仿制藥大國向創(chuàng)新藥強國的轉(zhuǎn)變。
近年來,制藥企業(yè)發(fā)起的注冊臨床試驗(industry sponsored trial, IST)是監(jiān)管部門批準新藥上市的主要依據(jù),但精心設(shè)計、良好組織實施的研究者發(fā)起的臨床研究(investigator-initiated clinical trials, IIT),對于支持新藥研發(fā)的積極推動作用越來越受到重視。由于IIT的設(shè)計、實施及質(zhì)量與IST存在差距,使得監(jiān)管部門、企業(yè)和研究者在利用IIT支持新藥研發(fā)時還存在顧慮。進一步了解存在的問題、分析面臨的挑戰(zhàn),進而提出解決策略,提高IIT的整體水平,將有助于推動IIT支持新藥研發(fā)。
1 IIT
國家衛(wèi)生健康委2021年9月9日發(fā)布《醫(yī)療衛(wèi)生機構(gòu)開展研究者發(fā)起的臨床研究管理辦法(試行)》中規(guī)定,IIT指醫(yī)療衛(wèi)生機構(gòu)開展的,以個體或群體(包括醫(yī)療健康信息)為研究對象,不以藥品醫(yī)療器械(含體外診斷試劑)等產(chǎn)品注冊為目的,研究疾病的診斷、治療、康復、預后、病因、預防及健康維護等的活動。由于IST是由企業(yè)出資發(fā)起,由企業(yè)主導,可能更傾向于得出有利于其產(chǎn)品的結(jié)論,而IIT往往來自于醫(yī)療實踐中產(chǎn)生的臨床問題,主要目標是學術(shù)和醫(yī)療管理,而不是商業(yè)目的,因此IIT可能比IST更為可信,其研究結(jié)果和發(fā)現(xiàn)不僅僅可以產(chǎn)生學術(shù)影響,推動制定醫(yī)療實踐指南,也可以在新藥研發(fā)中發(fā)揮重要作用。
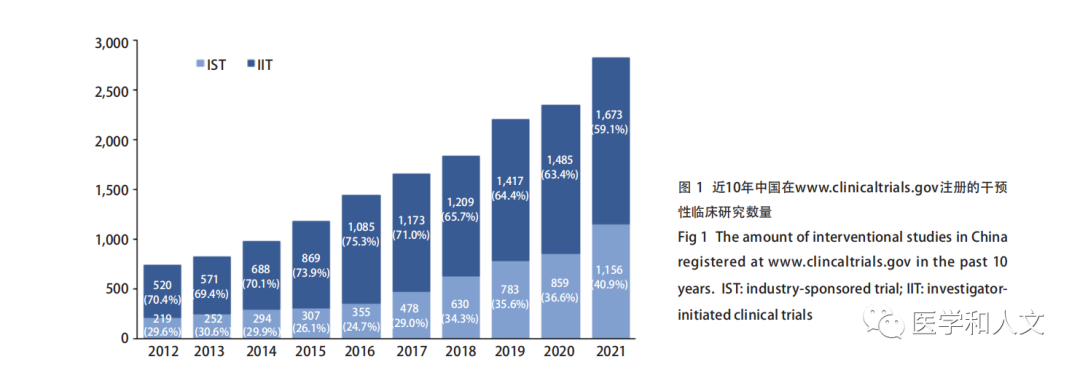
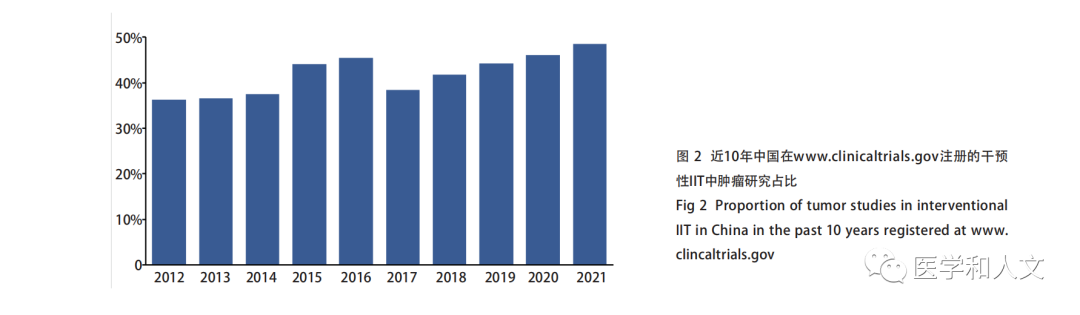
在www.clinicaltrials.gov網(wǎng)站上搜索2012年-2021年在中國開展的研究類型為Interventional Studies(Clinical Trials)的項目,基金來源于企業(yè)的作為IST,基金來源于美國衛(wèi)生研究院、美國政府、個人、大學、組織的作為IIT。結(jié)果發(fā)現(xiàn)10年間,IIT從520項增加到1,673項,占比波動于59.1%-75.3%(圖1),一定程度上反映了在我國IIT正在蓬勃開展的態(tài)勢。與近年來新藥研發(fā)的熱點集中在腫瘤領(lǐng)域一致,IIT研究中,腫瘤相關(guān)研究的占比高達36.3%-48.5%(圖2),且開展較多的適應(yīng)證多為我國的主要瘤種:肺癌、乳腺癌、食管癌、結(jié)直腸癌、胃/胰腺/壺腹部癌,說明IIT更貼近臨床,主要針對的是我國未被滿足的臨床需求。
2 IIT用于支持新藥研發(fā)
雖然在新藥研發(fā)領(lǐng)域,主要的臨床研究類型仍然是IST,但高質(zhì)量的IIT可以作為直接證據(jù)或重要的參考材料用于監(jiān)管部門新藥注冊(new drug application, NDA)審評,特別是作為支持批準新增適應(yīng)證的重要參考[3]。例如:歐洲藥品質(zhì)量管理局曾基于一項IIT的結(jié)果,批準美羅華擴展適應(yīng)證用于治療成人尋常型天皰瘡患者。在2021年美國食品藥品監(jiān)督管理局(Food and Drug Administration,FDA)基于1項IIT的數(shù)據(jù),批準普樂可復與其他免疫抑制性藥物聯(lián)用,預防接受肺移植的成人和兒科患者的器官排斥反應(yīng)。2018年中國國家食品藥品監(jiān)督管理局藥品審評中心(Center for Drug Evaluation, CDE)基于3項IIT提供的強有力的證據(jù),批準貝伐珠單抗聯(lián)合以鉑類為基礎(chǔ)的化療方案可用于晚期非鱗狀非小細胞肺癌的一線治療。
除了作為NDA的直接證據(jù)或參考材料,IIT還能為新藥研發(fā)提供方向、指導臨床試驗設(shè)計,或者作為基礎(chǔ)條件,支持關(guān)鍵注冊臨床試驗的方案設(shè)計、受試者人群選擇、樣本量估算等。在實施雙軌制管理的細胞治療領(lǐng)域,先于IST開展的IIT提供的材料,有助于獲得監(jiān)管部門對于新藥臨床試驗(investigational new drug, IND)的批準。例如:2022年5月,CDE基于一項IIT的研究結(jié)果,批準伊基侖賽注射液用于治療視神經(jīng)脊髓炎譜系疾病的臨床試驗申請。
IIT可以作為IST的補充,為新藥的IND與NDA提供支持性證據(jù),利用IIT研究上市后藥物拓展新的適應(yīng)證還可能降低新藥研發(fā)的費用[8],有助于控制藥費、降低疾病負擔。因此,應(yīng)當提倡開展高質(zhì)量IIT助力新藥研發(fā)。
3 存在的問題及挑戰(zhàn)
3.1 研究數(shù)量多、規(guī)模小、質(zhì)量參差不齊 國內(nèi)外的IIT普遍存在研究數(shù)量多、但規(guī)模小、質(zhì)量參差不齊,難以獲得高水平研究成果的情況[8-11]。2021年發(fā)表在《英國醫(yī)學雜志》的一項研究指出,2008年-2019年,中國大陸機構(gòu)發(fā)表了2,000多項他汀類藥物治療冠心病的IIT研究。這些研究只是簡單重復了藥物已知的療效,沒有得出任何新的有價值的研究結(jié)果。國內(nèi)一些針對IIT研究質(zhì)量的調(diào)查也發(fā)現(xiàn)IIT研究缺少成熟的研究團隊和充足的經(jīng)費支持,在研究方案設(shè)計、知情同意書簽署、研究過程中方案依從等方面均與IST有明顯差距。特別是,由于缺乏系統(tǒng)的監(jiān)查、稽查與核查,研究數(shù)據(jù)的可靠性、完整性存在一定的不確定性,研究結(jié)果遞交監(jiān)管部門時會面臨質(zhì)疑,甚至導致研究失敗。
3.2 研究者的方案設(shè)計能力和研究管理能力不足 部分IIT研究設(shè)計存在科學性問題甚至存在明顯的倫理挑戰(zhàn),研究結(jié)果難以用于支持NDA,主要原因是研究者的方案設(shè)計能力不足。大多數(shù)IST研究目的明確,申辦者企業(yè)有成熟的研究設(shè)計團隊,且方案經(jīng)過了CDE的審核,保證了研究設(shè)計的科學性。IIT的研究者為了解決臨床中發(fā)現(xiàn)的問題而設(shè)計研究,但由于臨床問題凝練不足、文獻檢索不充分、既往研究數(shù)據(jù)收集不完整,導致研究目的不明確或立項缺少充分論證和依據(jù)。部分IIT的研究者缺乏臨床研究的基本素養(yǎng),對于方案設(shè)計中的重要科學性要素缺乏把控能力,導致研究的對照設(shè)置、受試者人群選擇、研究藥物的劑量、療程、聯(lián)合治療方案的確定、主要療效指標、樣本量、統(tǒng)計學方法等關(guān)鍵設(shè)計缺乏科學性和嚴謹性。例如,腫瘤IIT研究中大量的單臂、聯(lián)合設(shè)計可能損害患者獲益并具有額外不可控風險。
IIT的研究者還存在研究管理能力不足的問題。主要研究者在日常繁忙的臨床工作之余常常無暇顧及臨床研究,其主要研究程序的執(zhí)行者和數(shù)據(jù)的收集者往往研究經(jīng)驗匱乏,合規(guī)意識不強,導致研究數(shù)據(jù)收集在及時性、準確性、完整性等方面存在缺陷。IIT研究中研究者風險意識薄弱,也沒有完整有效的風險控制體系,個別研究者對于受試者的保護關(guān)注不足,在研究過程中,對于不良事件的處理、報告不及時,退出終止研究的標準掌握不嚴格,應(yīng)當承擔的受試者補償不及時支付等情況也時有發(fā)生。
3.3 醫(yī)療機構(gòu)對于IIT的立項管理標準與IST不同 制藥企業(yè)發(fā)起的臨床試驗,經(jīng)藥監(jiān)部門批準后方可實施,研究過程及研究結(jié)果也受到嚴格的監(jiān)管。而研究者發(fā)起的臨床研究,衛(wèi)生行政主管部門尚未建立一整套行之有效的監(jiān)管策略,落實到醫(yī)療機構(gòu)內(nèi)對于IIT的監(jiān)管往往與IST標準不同。
目前醫(yī)療機構(gòu)對于IIT的管理大致分為兩種模式:IIT與IST管理標準相同或管理標準不同。IIT與IST同質(zhì)化管理可以保證對IIT的管理水平,但由于管理資源有限或者增加臨床研究數(shù)量等需要,目前采用這種管理模式的醫(yī)療機構(gòu)不多,IIT與IST管理標準不同的情況更為常見。IIT與IST由不同部門管理時往往IIT的管理更松,即便IIT與IST由同一部門管理,也有不少是資源向IST傾斜,而對IIT的重視程度不高,僅僅依靠主要研究者負責制,對于IIT的立項及研究質(zhì)量、數(shù)據(jù)安全、風險控制等缺少實質(zhì)性管理,立項管理和學術(shù)審查形同虛設(shè),有“失監(jiān)管”甚至”故意放水”的現(xiàn)象。更有甚者開展一些沒有明確的研究目的、不以解決臨床問題為導向,而是制藥企業(yè)出于占領(lǐng)市場的需要,打著IIT的幌子進行市場營銷的項目。
3.4倫理審查能力有待提高 根據(jù)目前的法規(guī)要求,開展IIT的醫(yī)療機構(gòu)必須設(shè)置倫理審查委員會,倫理委員會的規(guī)范性建設(shè)雖然有進步,但IIT的倫理審查能力不足仍然是目前比較突出的問題。IST倫理審查規(guī)范較為完善、審查嚴格、文件完整。即便如此,國產(chǎn)抗腫瘤藥物信迪利單抗在美國FDA申報上市被拒絕的原因體現(xiàn)出了我國臨床研究的倫理審查仍需進一步加強。與IST相比,IIT倫理審查工作尚處于起步階段,調(diào)查顯示IIT的倫理審查較為放松、更容易被批準。部分倫理委員會在初始審查中不能識別研究設(shè)計中挑戰(zhàn)倫理原則的問題,例如:對照組的選擇療效已明顯劣于患者可接受的可獲及治療、研究過程中對于不再獲益的受試者沒有設(shè)置合理的退出機制,研究的樣本量或統(tǒng)計學方法不合理而影響療效和安全性評估的可靠性等。而與初始審查相比,IIT的倫理跟蹤審查則更不規(guī)范甚至缺失。IIT研究的不良事件處理、受試者補償?shù)韧幢粋惱砦瘑T會嚴格監(jiān)管。由于存在潛在的倫理風險,利用IIT研究結(jié)果支持新藥研發(fā)上市也將面臨一定的挑戰(zhàn)。
3.5經(jīng)費不足 在我國IIT經(jīng)費來源大致有三類:政府設(shè)立的縱向課題;企業(yè)或基金會贊助;研究者自籌。我國醫(yī)學研究資助體系中,大多數(shù)針對基礎(chǔ)研究,對IIT的資助非常有限,而臨床研究的預算又往往較高。二者之間嚴重的不平衡整體呈現(xiàn)出IIT經(jīng)費不足的現(xiàn)象。由于研究經(jīng)費的不足,在研究設(shè)計上不得不做出一些妥協(xié),例如減少例數(shù)、刪減必要的檢查內(nèi)容或降低檢查的頻率、使用替代終點以縮短研究時間等。設(shè)計上的改變甚至將會影響研究結(jié)果的質(zhì)量。經(jīng)費不足還會導致實施過程中沒有足夠的團隊保證數(shù)據(jù)質(zhì)量,由于缺少交通補償可能導致受試者脫落,沒有必要的補償機制或賠償內(nèi)容不明確甚至帶來醫(yī)患糾紛等。
4 對策及建議
4.1 國家層面加強對IIT的監(jiān)管 盡管衛(wèi)健委頒布的《醫(yī)療衛(wèi)生機構(gòu)開展研究者發(fā)起的臨床研究管理辦法(試行)》已經(jīng)開始在北京、上海、廣東、海南四個省市進行試點,規(guī)范開展IIT的相關(guān)制度、政策特別是管理細則仍不明確,國家層面的監(jiān)督管理還亟待加強。應(yīng)當盡快通過試點總結(jié)出一套可普遍推廣的IIT管理要求,并且借鑒藥監(jiān)局臨床試驗數(shù)據(jù)核查的經(jīng)驗,開展IIT的質(zhì)量監(jiān)督檢查,提升醫(yī)療機構(gòu)及研究者對IIT的重視程度。對于沒有管理能力的醫(yī)療衛(wèi)生機構(gòu)和研究者,可以限制其開展用于支持新藥研發(fā)的IIT。
4.2 醫(yī)療機構(gòu)加強對于IIT的管理 IIT由于干預措施、經(jīng)費來源、研究者能力等不同導致項目的風險存在差異,管理難度也隨之加大。醫(yī)療機構(gòu)應(yīng)當成立專門的管理部門,制定相應(yīng)的管理制度規(guī)范,對研究者發(fā)起的臨床研究實施分類、嚴格、規(guī)范的管理。
支持新藥研發(fā)的IIT應(yīng)按照IST要求進行相應(yīng)的立項前的學術(shù)審查。學術(shù)委員會的審查范圍和審查能力應(yīng)當與開展的研究相匹配。除了本機構(gòu)內(nèi)的學術(shù)委員會,可以邀請機構(gòu)外的同行評議,還可以在立項前與CDE進行溝通交流,重點評估開展研究的前期基礎(chǔ)是否充分,研究設(shè)計是否合理等。
支持新藥研發(fā)的IIT必須嚴格遵守藥物臨床試驗質(zhì)量管理規(guī)范( good clinical practice, GCP),醫(yī)療機構(gòu)應(yīng)當使用與IST相同的質(zhì)量管理體系,必要時可以請獨立的第三方稽查協(xié)助提升研究質(zhì)量。質(zhì)控重點是可能嚴重影響研究結(jié)果的關(guān)鍵環(huán)節(jié)與關(guān)鍵數(shù)據(jù),包括研究中納入不符合入排標準的受試者、合并使用禁用藥物、關(guān)鍵訪視或重要觀察指標的缺失等。也要關(guān)注可能降低數(shù)據(jù)完整性和準確性的反復大量出現(xiàn)小的方案違背,例如檢查漏做、受試者漏服藥物、訪視超窗等。研究者既往研究經(jīng)驗少、病例登記和隨訪的支持系統(tǒng)不完備、入組病人數(shù)量非常多或非常少的項目,屬于研究質(zhì)量風險高的項目,還要予以特別關(guān)注。
4.3 提升倫理審查能力 IIT的倫理審查應(yīng)當實現(xiàn)與IST的同質(zhì)化管理,有條件的醫(yī)療機構(gòu)建議由同一個倫理委員會開展對IST和IIT的審查。項目比較多或確有必要分別由不同的倫理委員會審查時,應(yīng)當采用統(tǒng)一的管理體系,開展相同的培訓,并盡可能在不同倫理委員會中有一定的委員重疊,以保證所有倫理委員會的管理水平、審查能力和審查標準一致。
用于支持新藥研發(fā)的IIT,初始審查也應(yīng)當就研究的科學社會價值、臨床前研究和已完成的臨床研究的基礎(chǔ)、受試者人群的選擇、研究方案設(shè)計、研究的風險獲益以及受試者保護等因素進行充分審查。還必須根據(jù)風險程度落實研究過程中的跟蹤審查,特別對方案、知情同意書的修正、研究過程中的嚴重不良事件、方案偏離/違背等進行嚴格審查,以確保受試者的權(quán)益和研究結(jié)果的可靠,足以支持未來的注冊申請。
研究相關(guān)費用的支付及研究相關(guān)損害的診療和補償是受試者權(quán)益中的重要部分。IIT經(jīng)費來源不同,存在經(jīng)費支持不足的風險,倫理委員會應(yīng)切實在審查中履行受試者保護的職責。初始審查對于明顯經(jīng)費不足以支持開展的研究,不予批準。跟蹤審查時,重點關(guān)注對于研究過程中發(fā)生的嚴重不良事件的處理及應(yīng)當支付受試者的補償?shù)穆鋵嵡闆r。
4.4 提升研究者的能力 首先需要提升研究者的責任意識,研究者是臨床研究的核心,特別是在用于支持新藥研發(fā)的IIT中,研究者除了應(yīng)當承擔研究的實施、受試者的管理、研究數(shù)據(jù)的收集和結(jié)果的整理等責任,還需要承擔申辦者的部分甚至全部職責,包括設(shè)計研究方案、監(jiān)管研究質(zhì)量、報告不良反應(yīng)等。
應(yīng)當定期組織研究者培訓,培訓內(nèi)容應(yīng)當涵蓋研究方向梳理和科學問題凝練的能力、研究方案設(shè)計的能力、基本的流行病和統(tǒng)計學方法、臨床研究實施的法規(guī)和倫理學要求、相應(yīng)品種注冊臨床試驗的技術(shù)指導原則等。培訓應(yīng)當結(jié)合實際需要、要有針對性,還要反復多次開展,培訓后應(yīng)當以多種形式檢查培訓效果。
研究型醫(yī)院可以考慮搭建IIT的支撐平臺,提升對研究者的支持能力。配備研究型病房、中心藥房、相應(yīng)的信息化系統(tǒng)等,并由專職的研究支持人員為研究者提供研究資料檢索、方案設(shè)計、統(tǒng)計分析計劃、數(shù)據(jù)檔案管理、受試者管理等服務(wù)。必要時充分和制藥企業(yè)、監(jiān)管機構(gòu)以及其他醫(yī)療機構(gòu)建立多方聯(lián)系,共同協(xié)作管理研究風險。
4.5 保障研究經(jīng)費充足 IIT用于支持新藥研發(fā),當研究者的研究方向與企業(yè)的研發(fā)策略不相吻合,不能從制藥企業(yè)得到全額的經(jīng)費支持時,則需要更多源的經(jīng)費保障。由于歷史、制度、文化等原因,我國來自慈善基金、信托基金和個人捐款用于臨床研究的還非常少,應(yīng)當在監(jiān)管政策、輿論導向等方面進一步發(fā)力,引導學術(shù)組織、社會團體、基金會和個人等社會資金投向臨床研究。廣泛接受各種基金的資助,既可以有效緩解政府投入的不足,也可以規(guī)避由于過渡依賴企業(yè)資助,導致研究立題、過程實施、結(jié)果發(fā)布等環(huán)節(jié)受企業(yè)意愿的影響產(chǎn)生的偏倚。無論經(jīng)費來源于哪一方,都需要嚴謹?shù)暮贤瑮l款約定各方的責任和權(quán)利,也需要嚴格遵守利益沖突回避制度,從而保證經(jīng)費的使用合法、合規(guī)。
綜上所述,IIT對于支持新藥研發(fā)有重要價值,但IIT數(shù)量多、項目復雜、管理難度大。需要監(jiān)管部門、申辦方、研究機構(gòu)、倫理委員會和研究者共同提高對于IIT用于支持新藥研發(fā)作用的認識,深入了解研究機構(gòu)、研究項目、研究者的特點及管理復雜性,有針對性地采取解決措施,積極促進高質(zhì)量IIT的開展,以期更多高水平的研究成果用于解決未被滿足的臨床需求,推動新藥研發(fā)和上市。
參考文獻:略
