全文轉(zhuǎn)載自“iNature”微信公眾號
目前治療阿爾茨海默病相關(guān)癡呆的藥物可以暫時改善癥狀,但不能改變潛在的疾病進(jìn)程。可溶性和不可溶性淀粉樣β (Aβ)的積累可能啟動或增強阿爾茨海默病的病理過程。一些證據(jù)表明淀粉樣蛋白的去除可以減緩疾病的進(jìn)展一種抗淀粉樣抗體(aducanumab)已獲得美國食品和藥物管理局(FDA)的加速批準(zhǔn)。
Lecanemab是一種人源化單克隆抗體,與可溶性淀粉樣- β (a β)原纖維具有高親和力。已被證明對神經(jīng)元的毒性比單體或不可溶性原纖維更大,目前正在對早期阿爾茨海默病患者進(jìn)行測試。
2022年11月29日,在 New England Journal of Medicine 雜志在線發(fā)表題為“Lecanemab in Early Alzheimer’s Disease”的研究論文。該研究進(jìn)行了一項3期試驗(Clarity AD),以確定lecanemab在早期阿爾茨海默病參與者中的安全性和有效性。

Lecanemab是一種人源化IgG1單克隆抗體,與a β可溶性原纖維具有高親和力,目前正在對早期阿爾茨海默病患者進(jìn)行測試。一項涉及854名早期阿爾茨海默病患者的2b期劑量發(fā)現(xiàn)試驗,在12個月綜合評分變化(主要終點)的貝氏分析中,未顯示lecanemab與安慰劑之間存在顯著差異。然而,18個月時的分析顯示,使用lecanemab對淀粉樣蛋白的清除依賴于劑量和時間,并且該藥物在某些方面比安慰劑的臨床衰退更小。在該試驗中,每2周靜脈給予每公斤體重10 mg的lecanemab為適當(dāng)劑量,伴有水腫或積液(ARIA- e)的淀粉樣相關(guān)影像學(xué)異常(ARIA)發(fā)生率為9.9%(<3%有癥狀)。
該研究進(jìn)行了一項為期18個月、多中心、雙盲、三期試驗,試驗對象為50至90歲的早期阿爾茨海默氏癥患者(因阿爾茨海默氏癥導(dǎo)致的輕度認(rèn)知障礙或輕度癡呆),正電子發(fā)射斷層掃描(positron-emission tomography, PET)或腦脊液檢測顯示淀粉樣蛋白。受試者按1:1的比例被隨機分配靜脈注射lecanemab(每千克體重10毫克,每2周一次)或安慰劑。
該研究的主要終點是18個月時臨床癡呆方框評分(CDR-SB;范圍,0到18,分?jǐn)?shù)越高表示損傷越大)。關(guān)鍵的次要終點是PET上淀粉樣蛋白負(fù)擔(dān)的變化,阿爾茨海默病評估量表14項認(rèn)知亞量表的得分(ADAS-cog14;范圍,0到90;得分越高表示損傷越大),阿爾茨海默病綜合評分(ADCOMS;范圍,0到1.97;輕度認(rèn)知障礙的阿爾茨海默病合作學(xué)習(xí)-日常生活活動量表(ADCS-MCI-ADL;范圍,0到53;分?jǐn)?shù)越低,說明損傷越大)。
該研究最終將1795名參與者納入研究,其中898人接受lecanemab, 897人接受安慰劑。兩組患者基線時平均CDR-SB評分約為3.2。18個月時,與基線相比,lecanemab組調(diào)整后的最小二乘平均變化為1.21,安慰劑組為1.66(差異,?0.45;95%置信區(qū)間[CI],?0.67 ~?0.23;P < 0.001)。在一項涉及698名參與者的亞研究中,與安慰劑相比,lecanemab更能減少大腦淀粉樣蛋白負(fù)擔(dān)(差異,?59.1, loids;95% CI,?62.6 ~?55.6)。
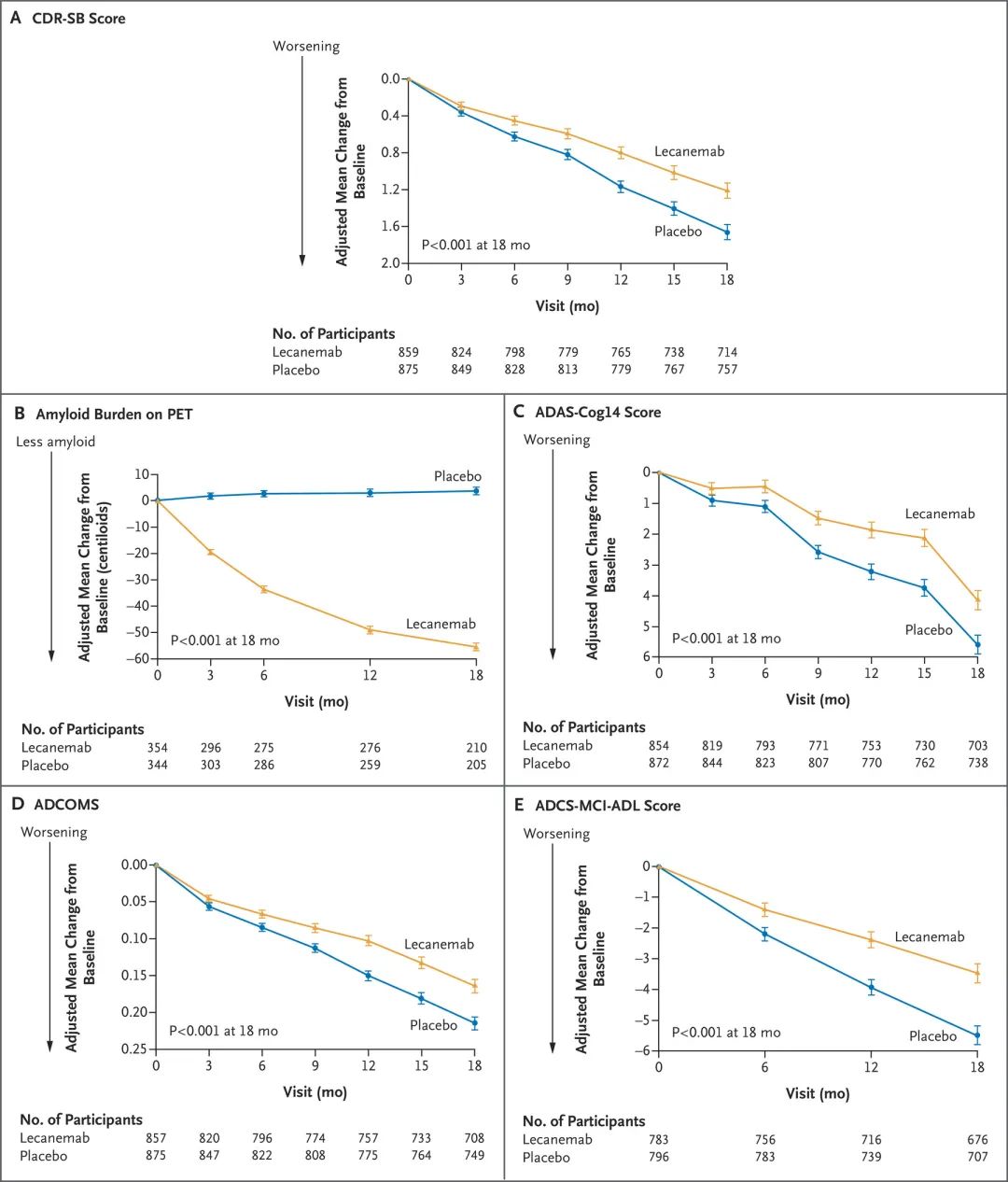
主要和關(guān)鍵的次要終點(圖源自 New England Journal of Medicine )
兩組患者從基線轉(zhuǎn)向lecanemab的其他平均差異如下:對于ADAS-cog14評分,?1.44 (95% CI,?2.27至?0.61;P < 0.001);對于ADCOMS,?0.050 (95% CI,?0.074 ~?0.027;P < 0.001);adc - mci - adl評分為2.0 (95% CI為1.2 ~ 2.8;P < 0.001)。Lecanemab導(dǎo)致26.4%的參與者出現(xiàn)灌注相關(guān)反應(yīng),12.6%的參與者出現(xiàn)淀粉樣蛋白相關(guān)影像學(xué)異常和水腫或積液。
綜上所述,該研究表明18個月時,Lecanemab降低了早期阿爾茨海默病的淀粉樣蛋白標(biāo)記物,與安慰劑相比,認(rèn)知和功能指標(biāo)的下降程度略有降低,但與不良事件有關(guān)。后續(xù)需要更長的試驗來確定lecanemab在早期阿爾茨海默病中的有效性和安全性。
原文鏈接:
DOI: 10.1056/NEJMoa2212948
